Hope • Science • Life
NRX-101
tutkimus, nopeasti alkanut ja jatkuva hoito kaksisuuntaiseen masennukseen potilailla, joilla on akuutti Itsetuhoajatus ja-käyttäytyminen
NRx: n tutkimuslääketieteellinen hoito NRX-100/NRX-101, jos Yhdysvaltain FDA ja muut terveysalan sääntelyvirastot hyväksyvät sen, olisi ensimmäinen lääkehoito, jota hoidetaan itsetuhoinen kaksisuuntainen mielialahäiriö. Nykyään mitään lääkettä ei ole hyväksytty kaksisuuntaista masennusta ja itsemurha-ajatuksia sairastavien potilaiden hoitoon ja ainoa FDA: n hyväksymä hoito tähän tappavaan tilaan on sähköhoito (ECT), jolla on hyvin tunnettuja haittavaikutuksia.
NRX-101 on patentoitu oraalinen kiinteäannosyhdistelmä kahdesta FDA: n hyväksymästä lääkkeestä: d-sykloseriini, NMDA-reseptorimodulaattori; ja Lurasidoni, 5-HT2a-reseptoriantagonisti, jolle FDA on myöntänyt Läpimurtohoitomerkinnän ja Erityisprotokollasopimuksen. NRX-101. Tuotteelle on myönnetty aineen koostumus-patentti, koska professori Daniel Javitt, MD, löysi synergistisen vaikutusmekanismin, jossa lääkkeen kahden komponentin nähdään kumoavan toistensa sivuvaikutukset laboratoriokokeissa. Tohtori Javitt kuuluu maailman siteeratuimpien tiedemiesten joukkoon ja oli ensimmäinen, joka tunnusti aivojen NMDA-reseptorin roolin psykiatrisissa sairauksissa vuonna 1987 ja on johtanut tätä neurokemian aluetta yli 600 tieteellisellä julkaisulla, joita on lainannut 46 000 ihmistä.
NMDA-antagonistilääkkeiden on viime aikoina laajalti tunnustettu hoitavan masennusta ja itsemurhaa. NMDA-kanavaa suoraan salpaavien aineiden, kuten ketamiinin ja dekstrometorfaanin, tiedetään kuitenkin aiheuttavan neurotoksisuutta (eli tappavan aivosoluja) ja aiheuttavan voimakasta riippuvuutta. NRX-101: n d-sykloseriinikomponentti ei ole osoittanut taipumusta neurotoksisuuteen tai riippuvuuteen (väärinkäyttövastuu) FDA: n vaatimissa standardilaboratoriokokeissa. NMDA-antagonistilääkkeillä on myös suuri potentiaali aiheuttaa hallusinaatioita, mikä tekee ketamiinista ja dekstrometorfaanista suosittuja väärinkäyttölääkkeinä. NRX-101-patentin taustalla oleva patentoitu löytö osoittaa osittain, että NRX-101: n lurasidonikomponentti estää D-sykloseriinin mahdollisuuden aiheuttaa hallusinaatioita laboratoriokokeissa, eikä hallusinaatioita ole havaittu yhdessä NRX-101: n kanssa ihmisillä tehdyissä kliinisissä tutkimuksissa.
FDA myönsi NRX-101: lle Breakthrough Therapy-nimityksen “Treatment of severe depression and acute suicidal ideation and behavior in patients with bipolar depression after first stabilization with ketamiini or other effective therapy.”NRX: n intitiaaliset vaiheen 3 tutkimukset NRX-101: llä kohdistuivat sekä ensihoidossa oleviin potilaisiin, joilla on aktiivinen itsemurha-ajatus ja jotka tarvitsevat ketamiinin (NRX-100) aloitusannoksen tilansa vakauttamiseksi, että myös avohoidossa hoidettaviin potilaisiin, joilla on vähemmän akuutti itsemurha-ajatus.
NRX-100/NRX-101: n mahdollisia kliinisiä etuja, joita tällä hetkellä tutkitaan kliinisissä tutkimuksissa, ovat:
- erityinen keskittyminen kaksisuuntaiseen masennukseen ASIB-potilailla: yli 50% kaksisuuntaista mielialahäiriötä sairastavista henkilöistä yrittää itsemurhaa elämänsä aikana.1 tällä hetkellä hyväksytyt lääkkeet on tarkoitettu vakavan masennuksen (MDD), Hoitoresistentin masennuksen (TRD) ja muiden masennuksen muotojen hoitoon.
- mahdollinen nopea Stabiloituminen potilailla NRX-100: n (ketamiini) kerta-annoksen jälkeen: vaiheittainen lääkehoito* vaatii vain yhden, ensimmäisen NRX-100: n (ketamiini) annostelun. Kliinisissä tutkimuksissa ketamiinilla on todettu nopeasti alkavia, masennuslääkkeitä / itsetuhoa ehkäiseviä vaikutuksia.2 ketamiini voi aiheuttaa dissosiatiivisia vaikutuksia (aistiharhoja); toistuva annostelu voi lisätä näitä dissosiatiivisia vaikutuksia entisestään..
- mukavuus: toisin kuin muut hoidot, NRX-101: tä kehitetään avohoidon mahdollistamiseksi NRX-100: n (ketamiini) tai muun tehokkaan hoidon alustavan vakauttamisen jälkeen.
NRX-101: n turvallisuusnäkökohdat ovat toistaiseksi rajoittuneet lievän sedaation, päänsäryn ja hypomanian havaittuihin sivuvaikutuksiin. Sekä D-sykloseriinilla että lurasidonilla on kuitenkin laajemmat sivuvaikutusprofiilit FDA: n hyväksymissä etiketeissä, ja nämä haittavaikutukset saattavat näkyä, kun useampia potilaita hoidetaan NRX-101: llä.
vaikutusmekanismi
NMDA säätelee ajatusten nopeutta:
liian vähäinen NMDA-aktiivisuus > lisääntynyt ajatus, hallusinaatiot, psykoosi
liian suuri NMDA-aktiivisuus > vähentynyt käsitys, masennus, itsemurha
NRX-101: n patentoitu kaksitoiminen vaikutusmekanismi kohdistuu NMDA – ja 5-HT2a-reseptoreihin-kaksi avainta reseptorit aivoissa.
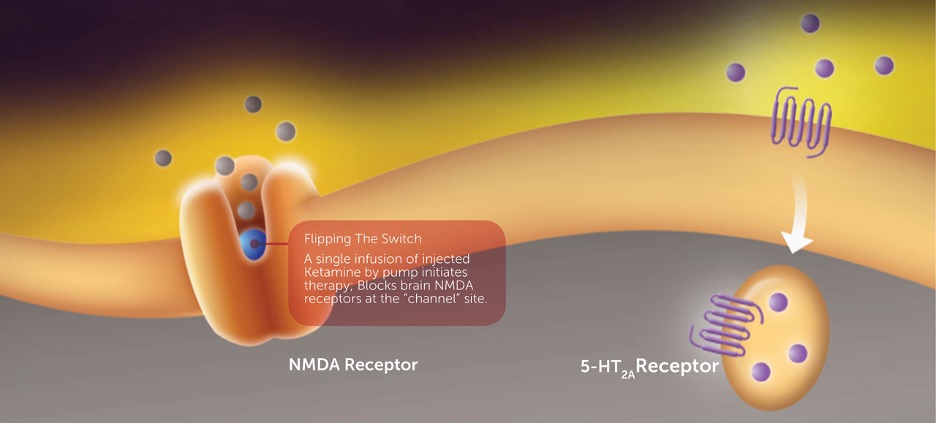
NMDA-reseptori on hermosoluissa esiintyvä glutamaattireseptori. Se on kriittinen muistin toiminnalle, koska se ohjaa signalointia hermosolusta hermosoluun. NMDA säätelee myös suoraan kalsiumionikanavaa, joka ohjaa aivojen ideaationopeutta (uusien ideoiden muodostumista). D-sykloseriini, yksi NRX-101: n vaikuttavista aineista, kohdistuu NMDA-reseptoriin ja moduloi NMDA-aktiivisuutta, mikä mahdollisesti edistää normaalia ajatustahtia. Useat ihmisillä tehdyt tutkimukset ovat osoittaneet, että D-sykloseriinin antaminen laukaisee masennuslääkkeen vaikutuksen. Meneillään oleva tutkimuksemme kuitenkin osoittaa, että hoito vaatii antipsykoottisen lääkkeen antamista psykomimeettisten sivuvaikutusten torjumiseksi.
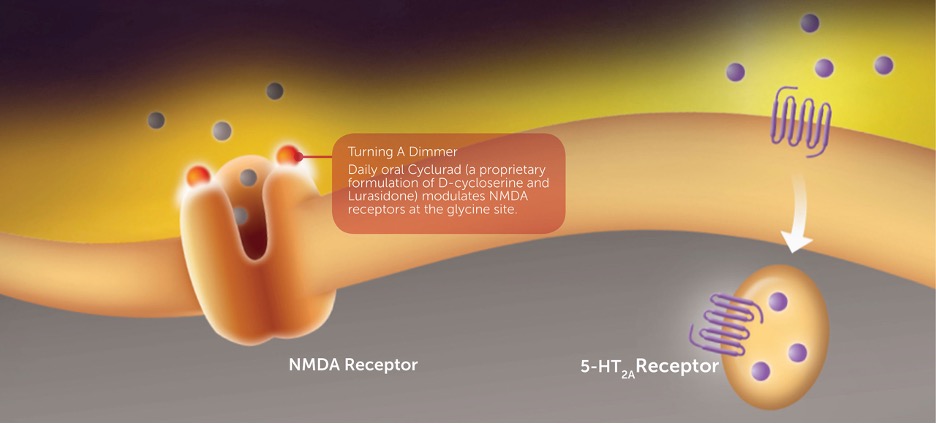
5-HT2a-reseptori on G-proteiinikytkentäinen reseptori ja serotoniiniperheen jäsen. Se tunnetaan roolistaan tiettyjen antipsykoottisten vaikutusten välittäjänä. Lurasidoni, NRX-101: n toinen vaikuttava aine, on 5-HT2a-antagonisti, joka on tällä hetkellä hyväksytty psykoosilääkkeeksi ja tarkoitettu kaksisuuntaisen mielialahäiriön hoitoon. Laboratoriotutkimukset ovat osoittaneet, että Lurasidonilla ja muilla 5-HT2a-antagonisteilla on odottamaton synergistinen vaikutus D-sykloseriinin kanssa, mikä saattaa voimistaa masennuslääkkeen vaikutusta ja vähentää mahdollisia psykomimeettisiä (hallusinaatioita) sivuvaikutuksia.
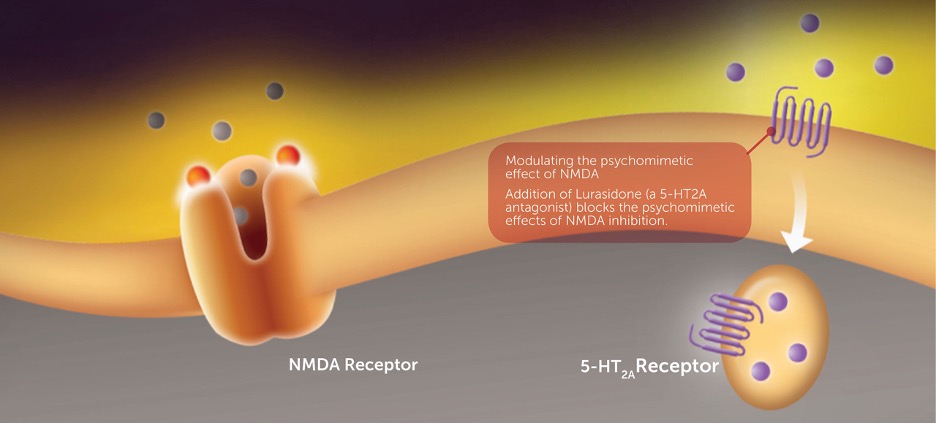
NRX-101: n patentoitu d-sykloseriinin ja Lurasidonin yhdistelmä on suunniteltu otettavaksi suun kautta päivittäin noin kuuden viikon ajan NRX-100: n (ketamiini) ensimmäisen kerta-infuusion jälkeen. Tämä terapeuttinen lähestymistapa voi tarjota suun kautta otettavaa avohoitoa, joka voi laajentaa merkittävästi NRX-100: n (ketamiinin) masennuslääkettä/itsetuhoa estävää vaikutusta.
kliiniset tiedot
täydelliset tulokset NRX: n STABIL-B-tutkimuksesta FDA Good Clinical Practices (GCP) – tutkimuksella tehty vaiheen 2 tutkimus esiteltiin American College of Neuropsychopharmacology-yliopistossa joulukuussa 2019. Yhdysvaltain elintarvike-ja lääkevirasto myönsi Break Therapy-nimityksen (BTD) NRX-101: lle tämän tutkimuksen perusteella.
BTD on prosessi, jonka tarkoituksena on nopeuttaa sellaisten lääkkeiden kehittämistä ja tarkistamista, jotka on tarkoitettu vakavan sairauden hoitoon, ja alustavat kliiniset todisteet osoittavat, että hoito voi osoittaa merkittävää paranemista saatavilla oleviin lääkkeisiin verrattuna kliinisesti merkittävissä päätepisteissä.
tässä tutkimuksessa 20 potilasta, jotka tuotiin ensiapuun ja joilla oli vaikea kaksisuuntainen mielialahäiriö ja akuutti itsemurha-ajatus, stabiloitiin aluksi yhdellä ketamiini-infuusiolla laskimoon (NRX-100). Tutkimuksen yksityiskohdat voidaan nähdä www.clinicaltrials.gov.3
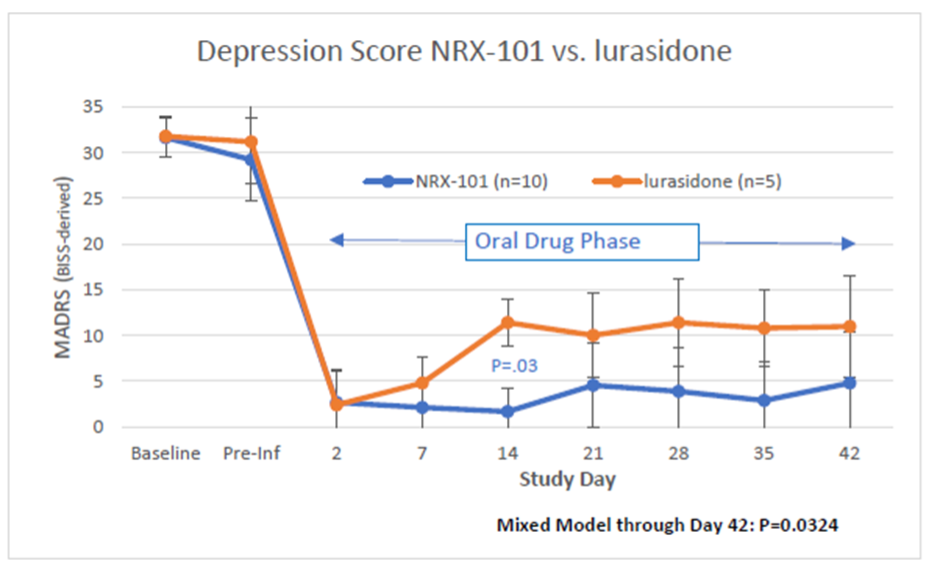
stabiloinnin jälkeen potilaat satunnaistettiin (2: 1) joko NRX-101-hoitoon tai pelkkään lurasidonihoitoon masennuksen ja itsetuhoajatusten aiheuttaman remission ylläpitämiseksi. Kuten alla olevasta top-line-analyysistä käy ilmi, NRX-101-hoitoa saaneilla masennustaso oli 14 päivän kohdalla merkitsevästi alhaisempi kuin lurasidonia saaneilla (P=0, 03). Suuntaus jatkui 42 päivän ajan (P=0, 032).
Lurasidonilla hoidetuista kontrollipotilaista 2/5: llä havaittiin relapsia joko masennuksessa tai itsemurhassa, kun taas NRX-101: llä hoidetuilla potilailla relapsia ei havaittu (P=.095). Tutkimuksen oraalisessa lääkevaiheessa ei havaittu lääkkeeseen liittyviä vakavia haittatapahtumia eikä hallusinaatioita. Nämä tiedot eivät muodosta kummankaan hoitoryhmän täyttä turvallisuusprofiilia kliinisessä tutkimuksessa.
aiemman tutkimuksen tulokset julkaistiin Journal of Clinical Psychiatry-lehdessä vuonna 2015. Tässä tutkimuksessa kaksisuuntaista mielialahäiriötä sairastavat potilaat, jotka saivat jo 5-HT2a-antagonistia, saivat yhden ketamiinikuution laskimoon ja sen jälkeen päivittäisen, suun kautta otettavan d-sykloseriinin. Tulokset osoittivat, että masennusoireet vähenivät >50% ja itsemurha-ajatukset vähenivät 75%. Näillä potilailla terapeuttinen vaikutus säilyi vähintään kahdeksan viikkoa.
Prekliiniset tiedot osoittavat, että lurasidonin (ja muiden 5ht2a-antagonistien) ja D-sykloseriinin yhdistelmä vähensi akatisiaa merkittävästi kontrolliryhmään ja pelkkään lurasidoniin verrattuna. Nämä löydökset on kuvattu yksityiskohtaisesti useissa Yhdysvaltain ja Yhdysvaltain entisissä patenttihakemuksissa. Akatisia määritellään kiihtymyksen, ahdistuksen ja levottomuuden tilaksi, joka on antipsykoottisten ja masennuslääkkeiden satunnainen sivuvaikutus.
- Pallaskorpi ym. Kaksisuuntainen mielialahäiriö 2017; 19: 13-22
- Zarate, C. et al. Biologinen Psykiatria 2012; 71(11); 939-946
- https://www.clinicaltrials.gov/ct2/show/NCT02974010?term=stabil-b&rank=1
- Kantrowitz, et al: J kliininen Psykiatria 2015; 76(6): 737-738
Leave a Reply