a fenolftalein indikátor színe bázikus oldatban: (a) sárga(B) Zöld(C) Rózsaszín (D) Narancs
tipp: a fenolftalein gyenge sav, ezért oldatban ${H^ + }$ ionokat szabadít fel. Az anion így színes formában képződik, és jelzi a végpontot. Ha bázist adunk a fenolftaleinhez, az egyensúly a savas közeg felé tolódik el, és több ${H^ + }$ iont szabadít fel.
teljes lépésről lépésre megoldás:
– a fenolftalein egy szintetikus indikátor, amelynek molekuláris képlete ${C_{20}}{H_{14}}{O_4}$. A festékek ftalein osztályába tartozik, és leggyakrabban a sav-bázis titrálások indikátoraként használják. Természeténél fogva nagyon alacsony a vízben való oldhatósága, ezért kísérletekben való felhasználásra alkoholban oldódik.
szerkezete:
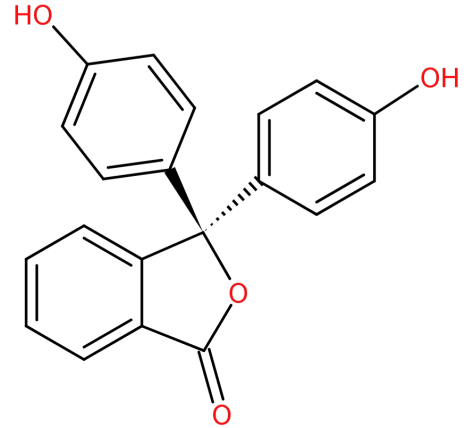
-a ftálsav-anhidrid két ekvivalens fenollal történő kondenzációjával keletkezik savas körülmények között.
– ez egy gyenge sav, így képes elveszíteni ${H^+} $ ionokat az oldatban. A ${H^ + }$ ion elvesztése előtt a fenolftalein molekula színtelen, de a ${H^ + }$ ion elvesztése után a fenolftaleinion képződik, amely rózsaszínű.
Le-Chatelier elve szerint, ha bázist adunk a fenolftaleinhez, az egyensúly a savas közeg felé tolódik el, ami több ${H^ + }$ ion felszabadulását eredményezi. Így az oldat színtelenről rózsaszínre változik.
ezért azt mondhatjuk, hogy a fenolftalein színtelen marad savas és semleges oldatokban, és bázikus oldatokban rózsaszínűvé válik. 8-as pH-értékig színtelen marad.5, míg ezen felül rózsaszínből mélyvörösre változik.
– folyékony állapotban színtelen, de szilárd kristályos formában a fenolftalein sárgásfehér vagy halvány narancssárga vagy finomfehér kristályos por.
– a fenolftaleint széles körben használják pH indikátorként és laboratóriumi szerként. Azt is használják a sav-bázis titrálás indikátorként, gyógyszerileg, mint egy hashajtó és Kastle-Mayer teszt is. A metilvörös, a timolkék és a bróm-timol kék mellett az univerzális indikátor komponenseként is működhet.
tehát a helyes opció: (C) Rózsaszín.
Megjegyzés: A pH-változások miatt vizes oldatokban akár 4 különböző állapotot is képes elfogadni. Ha a körülmények erősen savasak, protonált formában létezik ($H{\ln^+}$), amelynek narancssárga színe van. Erősen savas és enyhén lúgos körülmények között lakton formában (HLN) létezik, amely színtelen. Alapvető körülmények között kétszeresen deprotonált fenolát formában létezik (${\ln ^{2 -}}$), amely színtelen, erősen bázikus körülmények között pedig $\ln {(OH)^{3 – }}$ formát képez, amely színtelen.
Leave a Reply