fargen på fenolftaleinindikatoren i grunnoppløsning er:(A) Gul(B) Grønn(C) Rosa(D) Oransje
Hint: Fenolftalein er en svak syre og så frigjør den ${H^ + }$ ioner i oppløsning. Anionen danner således i farget og indikerer endepunktet. Å legge til en base til fenolftalein fører til at likevekten skifter mot det sure medium og frigjør mer ${H^+} $ ioner.
Komplett trinnvis løsning:
-Fenolftalein er en syntetisk indikator med en molekylformel på ${C_{20}}{H_{14}}{O_4}$. Det tilhører ftaleinklassen av fargestoffer og brukes oftest som indikator i syrebasetitreringer. Av natur har den svært lav oppløselighet i vann og så for bruk i eksperimenter, er den oppløst i alkohol.
dens struktur er:
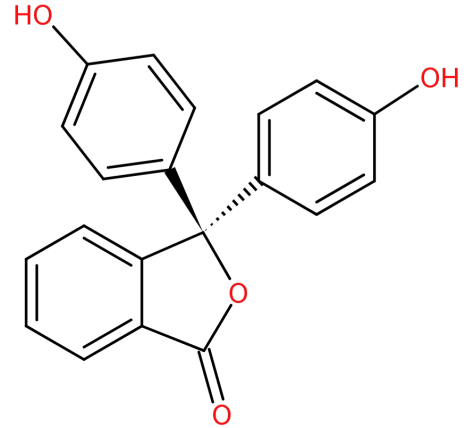
-den dannes ved kondensering av ftalanhydrid med to ekvivalenter av fenol under sure forhold.
– det er en svak syre og så har evnen til å miste ${H^+} $ ioner i oppløsning. Før du mister ${H^ + }$ ion, er fenolftaleinmolekylet fargeløst, men etter å ha mistet ${H^ + }$ ion danner det fenolftaleinionet som er rosa i farge.
Ifølge Le-Chateliers prinsipp, hvis vi legger til en base for fenolftalein, vil likevekten skifte mot surt medium som fører til frigjøring av flere ${H^ + }$ ioner. Dermed snu oppløsningen fra fargeløs til rosa.
derfor kan vi si at fenolftalein forblir fargeløs i sure og nøytrale løsninger og blir rosa i grunnleggende løsninger. Den forblir fargeløs til pH på 8.5, mens over at det blir rosa til dyp rød i fargen.
– i flytende tilstand er den fargeløs, men når den finnes i fast krystallinsk form, er fenolftalein gulaktig-hvitt til blekoransje eller fint hvitt krystallinsk pulver.
-Fenolftalein er mye brukt som en ph-indikator og et laboratoriemiddel. Det er også brukt i syre-base titreringer som en indikator, medisinsk som et avføringsmiddel og I Kastle-Mayer test også. Sammen med metylrød, tymolblå og bromotymolblå, kan den også fungere som en komponent i universell indikator.
så det riktige alternativet vil være: (C) Rosa.
Notat: Det kan vedta opptil 4 forskjellige tilstander i vandige løsninger på grunn av pH-endringene. Når forholdene er sterkt sure, eksisterer det i protonert form ($H{\ln^+}$), som har oransje farge. Når forholdene er mellom sterkt sure og litt grunnleggende, finnes det i laktonform (Hln) som er fargeløs. Under grunnleggende forhold eksisterer den som dobbelt deprotonert fenolatform (${\ln ^{2 -}}$) som er fargeløs og under sterkt grunnleggende forhold danner den $\ln {(OH)^{3 – }}$ form som er fargeløs.
Leave a Reply