A cor do indicador fenolftaleína em solução básica é:(A) Amarelo(B), Verde(C) cor-de-Rosa(D) Laranja
Dica: Fenolftaleína é um ácido fraco e então ele libera ${H^ + }$ íons em solução. O ânion, portanto, se forma em cores e indica o ponto final. Adicionar uma base à fenolftaleína faz com que o equilíbrio mude para o meio ácido e libere mais íons ${H^+}$.
Solução Passo a passo completa:
-a fenolftaleína é um indicador sintético com uma fórmula molecular de ${C_{20}} {H_{14}} {o_4}$. Pertence à classe de corantes de ftaleína e é mais frequentemente usado como um indicador em titulações ácido-base. Por natureza, tem muito baixa solubilidade em água e, portanto, para uso em experimentos, é dissolvido em álcool.
Sua estrutura é:
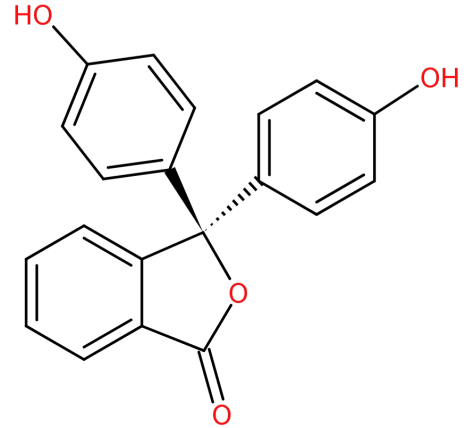
-Ele é formado pela condensação do anidrido ftálico com dois equivalentes de fenol sob condições ácidas.
– é um ácido fraco e, portanto, tem a capacidade de perder íons ${H^ + }$ em solução. Antes de perder o íon $ {h^+}$, a molécula de fenolftaleína é incolor, mas depois de perder o íon ${h^+}$, ela forma o íon fenolftaleína de cor Rosa.De acordo com o princípio de Le-Chatelier, se adicionarmos uma base à fenolftaleína, o equilíbrio mudará para o meio ácido, levando à liberação de mais íons ${H^+}$. Assim, transformando a solução de incolor em rosa.Portanto, podemos dizer que a fenolftaleína permanece incolor em soluções ácidas e neutras e fica rosa em soluções básicas. Permanece incolor até pH de 8.5, enquanto acima disso, torna-se rosa para vermelho profundo na cor.
-no estado líquido, é incolor, mas quando encontrado na forma cristalina sólida, a fenolftaleína é branco-amarelada a laranja pálido ou pó cristalino branco fino.
– a fenolftaleína é amplamente utilizada como indicador de pH e agente laboratorial. Também é usado em titulações ácido-base como indicador, medicinalmente como laxante e no teste de Kastle-Mayer também. Junto com o vermelho metílico, o azul do timol e o azul do bromotimol, pode igualmente actuar como um componente do indicador universal.
então, a opção correta será: (C) Rosa.
Nota: Pode adotar até 4 estados diferentes em soluções aquosas devido às mudanças de pH. Quando as condições são fortemente ácidas, existe na forma protonada ($H{\ln ^ + }$), que tem coloração laranja. Quando as condições estão entre fortemente ácidas e ligeiramente básicas, existe na forma de lactona (Hln) que é incolor. Sob condições básicas, existe como forma fenolada duplamente desprotonada (${\ln ^{2 – }}$) que é incolor e sob condições fortemente básicas forma $\ln {(OH)^{3 – }}$ forma que é incolor.
Leave a Reply