färgen på fenolftaleinindikatorn i basic solution är:(A) gul(B) grön(C) Rosa(D) Orange
tips: fenolftalein är en svag syra och så släpper den ${H^ + }$ joner i lösning. Anjonen bildas således i färgad och indikerar slutpunkten. Att lägga till en bas till fenolftalein får jämvikten att växla mot det sura mediet och frigöra mer ${H^ + }$ joner.
komplett steg för steg lösning:
-fenolftalein är en syntetisk indikator med en molekylformel på ${C_{20}}{H_{14}}{O_4}$. Det tillhör ftaleinklassen av färgämnen och används oftast som en indikator i syrabastitreringar. Av natur har den mycket låg löslighet i vatten och så för användning i experiment löses den i alkohol.
dess struktur är:
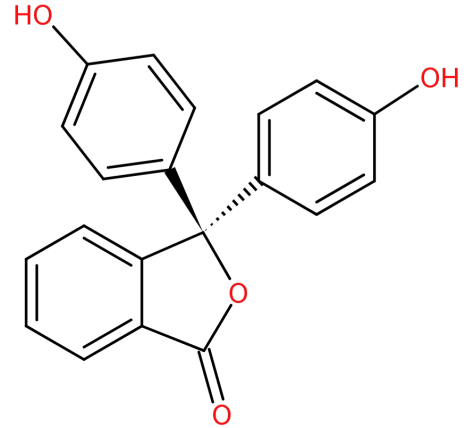
-det bildas genom kondensation av ftalsyraanhydrid med två ekvivalenter av fenol under sura betingelser.
– det är en svag syra och så har förmågan att förlora ${H^ + }$ joner i lösning. Innan du förlorar ${H^ + }$ Jon, är fenolftaleinmolekylen färglös men efter att ha förlorat ${H^ + }$ Jon bildar den fenolftaleinjonen som är rosa i färgen.
enligt Le-Chateliers princip, om vi lägger till en bas till fenolftalein, kommer jämvikten att skifta mot surt medium som leder till frisättning av mer ${H^ + }$ joner. Således vänder lösningen från färglös till rosa.
därför kan vi säga att fenolftalein förblir färglös i sura och neutrala lösningar och blir rosa i basiska lösningar. Det förblir färglöst till pH på 8.5, medan ovanför det blir rosa till djupröd i färg.
– i flytande tillstånd är det färglöst men när det finns i fast kristallin form är fenolftalein gulvitt till blekorange eller fint vitt kristallint pulver.
-fenolftalein används ofta som en pH-indikator och ett laboratoriemedel. Det används också i syrabastitreringar som en indikator, medicinskt som laxermedel och i Kastle-Mayer-test också. Tillsammans med metylröd, tymolblå och bromotymolblå kan den också fungera som en komponent i universell indikator.
så det rätta alternativet blir: (C) Rosa.
notera: Det kan anta upp till 4 olika tillstånd i vattenhaltiga lösningar på grund av pH-förändringarna. När förhållandena är starkt sura finns det i protonerad form ($H{\ln ^ + }$), som har orange färgning. När förhållandena är mellan starkt sura och något basiska finns det i laktonform (Hln) som är färglös. Under grundläggande förhållanden existerar den som dubbelt deprotonerad fenolatform (${\ln ^{2 – }}$) som är färglös och under starkt grundläggande förhållanden bildar den $\ln {(OH)^{3 – }}$ form som är färglös.
Leave a Reply